Останніми роками цироз печінки значно помолодшав. А справа в тому, що фіброз, який призводить до цієї смертельної хвороби, майже не має симптомів. Отже, лише вчасна діагностика може врятувати життя пацієнта.
Сучасна медицина володіє чималою кількістю діагностичних методів – від механічних до біохімічних. Проте обрати той, що дасть максимально правдивий результат у конкретного пацієнта – завдання з багатьма невідомими. Вирішити його допоможе доцент кафедри сімейної медицини і терапії УМСА, кандидат медичних наук Ігор Іваницький.
Чим небезпечний фіброз печінки?
 Ігор ІВАНИЦЬКИЙ, доцент кафедри сімейної медицини і терапії УМСА, кандидат медичних наук
Ігор ІВАНИЦЬКИЙ, доцент кафедри сімейної медицини і терапії УМСА, кандидат медичних наукФіброз печінки – це розвиток великого обсягу сполучної тканини внаслідок занадто активного відновлення тканини печінки. Сутність фіброзу складає надмірно високе утворення позаклітинного матриксу та його неповна деградація. Початковим фактором розвитку є хронічне запалення паренхіми печінки, особливо при персистуючому перебігу. Фіброзні зміни печінки зазвичай не викликають симптомів, але можуть призводити до розвитку портальної гіпертензії, оскільки змінюють мікроциркуляцію в печінковій паренхімі, або до розвитку цирозу (ділянки фіброзу змінюють нормальну мікроструктуру печінкової тканини і, як наслідок, викликають дисфункцію печінки).
Причини, що викликають фіброзні зміни печінки
Фіброзні зміни печінки можуть бути викликані різними причинами. Серед них слід виділити хронічні гепатити, які можуть мати вірусну (вірусні гепатити В,С), бактеріальну (бруцельоз) або паразитарну (ехинококоз, опісторхоз) етіологію. Можливою причиною є токсичні впливи на печінку як немедикаметозного (алкоголь), так і медикаметозного (аміодарон, хлорпромазин, ізоніазід, метотрексат, метилдопа) генезу. У списку причин розвитку фіброзу також аутоімунний гепатит, деякі хвороби накопичення та вроджені порушення метаболізму.
У той же час, найбільш частою причиною розвитку фіброзу печінки залишається стеатогепатит як алкогольного, так і неалкогольного генезу. Патофізіологія розвитку цього стану включає накопичення жиру (стеатоз), хронічне запалення і, як, наслідок, фіброз.
Стеатоз – це результат накопичення тригліцеридів у гепатоцитах. Можливі механізми розвитку стеатозу: зниження синтезу ліпопротеїнів дуже низької щільності і підвищення синтезу печінкових тригліцеридів (можливо, за рахунок зниження окислення жирних кислот або підвищення кількості вільних жирних кислот, що надходять в печінку). Запалення виникає внаслідок перекисного окислення ліпідів, що викликає пошкодження клітинних мембран. Такі зміни можуть стимулювати стеллатні клітини печінки, що в результаті призводить до фіброзу.
Одноразовий шкідливий вплив на печінку (наприклад, гострі токсичні гепатити, гепатит А), навіть при дуже важкому перебігу, зазвичай не впливає на мікроархітектоніку і не супроводжується фіброзними змінами, навіть за умови масової загибелі гепатоцитів. На ранніх стадіях фіброзні зміни печінки можуть регресувати, якщо причина усунена (наприклад, при виключенні токсичних чинників). За умови тривалого впливу шкідливих факторів, на фоні хронічного запалення фіброзні зміни стають постійними. Необхідно враховувати, що наявність обструкції жовчновивідних шляхів призводить до швидкого прогресування фіброзу.
Для різних причин розвитку цього захворювання характерні різні типи фіброзу
Венулярний і перівенулярний фіброз, який розвивається в центрі часточок, можливий на фоні хронічного гепатиту алкогольного генезу, на фоні застойних змін, обумовлених серцево-судинною патологією.
Перицелюлярний фіброз(навколо гепатоцитів) спостерігається при хронічних вірусних гепатитах і захворювання печінки алкогольної етіології.
Септальний фіброз – патологія, яка виникає після масової загибелі клітин печінки. Ділянки фіброзу, або септи, з’єднують між собою портальні вени (порто-портальні септи) або портальні вени і центральні вени (порто-центральні септи), внаслідок чого розвивається порушення нормальної будови печінки. У септах розвиваються судини-анастомози, які безпосередньо поєднують гілки ворітної вени і печінкової артерії з печінковими венами, оминаючи функціонально-активну паренхіму печінки.
Портальний і перипортальній фіброз є типовими для хронічного перебігу гепатиту різної етіології (вірусної, алкогольної, аутоімунної).
Перідуктальний фіброз зазвичай характеризується розростанням фіброзної тканини навколо протоків жовчновивідної системи. Може розвиватись на фоні склерозуючого холангіту і має важливе значення для ранньої діагностики.
Найчастішою формою фіброзу є змішана, коли у різних пропорціях поєднуються різні форми фіброзу.
Як оцінюються ступені фіброзних змін
На сьогоднішній день найчастіше застосовуються декілька систем оцінки ступеня фіброзу:МЕТАVIR, Knodell, Ishak. Кінцевою метою при використанні цих шкал є отримання універсального клінічно значимого показника, який дає можливість комплексно відобразити всі ознаки (локалізацію, поширеність, ступінь вираженості) ураження печінкової тканини. Основною проблемою при використанні цих шкал стає відсутність жорсткого розмежування між фіброзними змінами печінкової тканини з одного боку і змінами, обумовленими активністю процесу і некро-запальними змінами – з іншого, що може призводити до неоднозначної оцінки стану пацієнта.
Однією з найбільш розповсюджених та найбільш широко уживаних в практичній медицині шкал фіброзу печінки є шкала METAVIR, яка має наступні градації:
- F0: фіброз відсутній;
- F1: портальний і перипортальній фіброз без утворення септ;
- F2: портальний і перипортальній фіброз з одиничними септами;
- F3: портальний і перипортальний фіброз з множинними септами;
- F4: цироз.
Однією із особливостей шкали METAVIR є наявність підшкали некрозапальної активності, яка визначає пошкодження при портальному запаленні і гепатоцелюлярному некрозі.
За шкалою METAVIR виділяється 4 стадії активності:
- A0: активність відсутня;
- A1: мінімальна активність;
- A2: помірна активність;
- A3: висока активність.
Симптоми фіброзу, який не має власних симптомів
Однією із основних особливостей перебігу фіброзу печінки є те, що сам по собі він не викликає симптомів. Симптоми можуть бути результатом основного захворювання, що викликало розвиток фіброзу, або результатом ускладнень портальної гіпертензії у разі переходу фіброзу в цироз.
Ці симптоми включають в себе жовтяницю, кровотечі з варикозно змінених вен стравоходу, асцит і портосистемну енцефалопатію. Цироз може призвести до розвитку печінкової недостатності, яка є потенційно смертельною.
Циротичні зміни печіки зазвичай можне без великих проблем виявити за допомогою ультразвукового обстеження. Для цирозу характерні збільшення або зменшення лінійних розмірів, виражена неоднорідність ехоструктури, бугристість контурів, притуплення кутів, розширення портальної вени, що зазвичай свідчить про приєднання портальної гіпертензії.
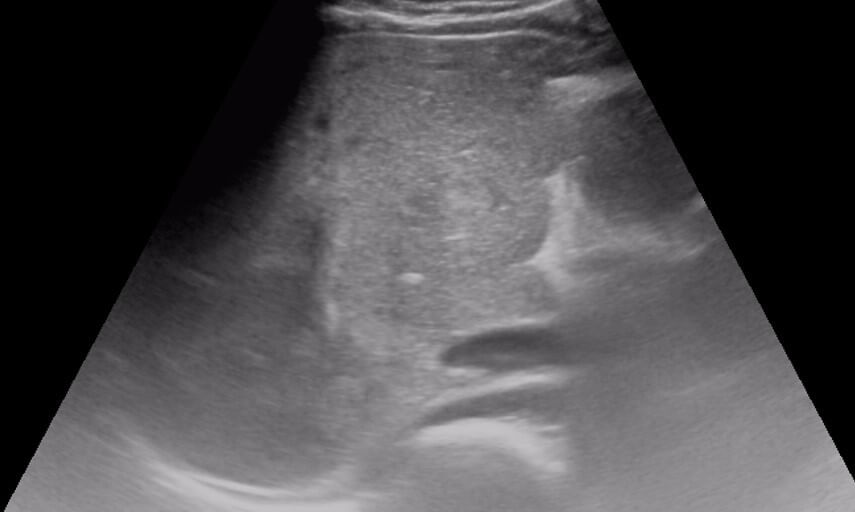
На жаль, на тому етапі, коли у пацієнта можна виявити перелічені ознаки, можливість ефективної допомоги зводиться до трансплантації печінки, тому одним із найбільш проблемних питань залишається раннє виявлення фіброзу та оцінка його ступеня.
Діагностика фіброзу печінки методом біопсії
Золотим стандартом діагностики фіброзу при хронічному гепатиті тривалий час вважалося гістологічне дослідження біоптатів печінки. Результати дослідження дозволяють:
- визначити етіологію хронічного гепатиту, ступінь його активності та стадію процесу;
- встановити наявність цирозу печінки, диспластичних змін гепатоцитів;
- виявити гепатоцелюлярну карциному;
- прогнозувати перебіг захворювання та ефективність терапії;
- оцінити результати противірусної терапії при повторних біопсіях.
Однак щодо доцільності біопсії саме для визначення стадії фіброзу печінки немає єдиної думки. Деякі автори вважають, що далеко не кожному хворому із хронічним вірусним гепатитом або цирозом печінки показана черезшкірна пункційна біопсія печінки – для її проведення необхідно мати чітко аргументовані показання, оскільки можливості біопсії обмежені погрішностями при отриманні матеріалу, неоднозначністю трактування результатів, ризиком ускладнень аж до летальних випадків, а також безліччю протипоказань. Також необхідно враховувати, що для оцінювання стану печінкової тканини в динаміці або для визначення ефективності проведеного лікування будуть потрібні повторні біопсії. Окремою проблемою є також висока вартість цього дослідження.
Найбільш частим варіантом біопсії є трепанобіопсія. Методика дозволяє отримати стовпчик тканини для гістологічного дослідження, що важливо насамперед в діагностиці дифузної патології. У трепанобіопсії печінки використовується спеціальна голка. Зазвичай вона складається з внутрішньої і зовнішньої частин, де виставляється довжина стовпчика матеріалу біопсії: 1, 1,5 або 2 см. При спрацьовуванні зовнішня частина голки «зрізає» біопсійний стовпчик діаметром зі звичайну нитку, зберігаючи цілісність матеріалу для подальшого дослідження. «Сліпа» пункція такими голками небажана в зв’язку з високим ризиком розвитку ускладнень. Обов’язковою умовою виконання процедури є ультразвукова візуалізація в режимі реального часу з використанням доплерографії, що дозволяє обирати безпечну траєкторію пункційного каналу. Трепанобіопсія печінки при дифузних її ураженнях (гепатит, в т.ч. вірусний, цироз) голкою 16 G і довжиною 150 мм дозволяє отримати матеріал, який повністю відповідає міжнародним гістологічним стандартам. У момент введення голки хворий затримує дихання на повному видиху (з метою мінімізації ушкодження). Вся процедура проводиться під місцевою анестезією протягом 15 хвилин. За цей час в 7-му сегменті правої частки печінки набираються три біопсійні стовпчики. Необхідною умовою виконання процедури є подальше спостереження за пацієнтом в динаміці протягом 24 годин з обов’язковим ультразвуковим контролем.
Абсолютними протипоказаннями до проведення біопсії печінки є некомпенсовані порушення в системі згортання крові (протромбін <60%, кількість тромбоцитів <60.000 / мкл або час кровотечі> 10 хвилин), підозри на наявність кісти, гемангіоми або іншої пухлини з підвищеною васкуляризацією. Відносно протипоказана біопсія при значному асциті і наявності вогнищ інфекції в плевральній порожнині та піддіафрагмальному просторі. У цих випадках більш оптимальним є лапароскопічне дослідження.
Ускладнення після біопсії печінки виникають вкрай рідко, а летальність становить менше 0,01%. 96% всіх ускладнень спостерігаються в перші 24 години, а 60% з них – в перші 2 години після процедури. До найбільш серйозних ускладнень належать кровотечі в черевну порожнину, в тканину або під капсулу печінки і гемобілія. Формування артеріо-венозної фістули і незначні внутрішньопечінкові гематоми зазвичай протікають безсимптомно і не мають клінічного значення. Близько чверті хворих відчувають кілька годин після процедури ниючий біль в місці пункції, якого легко позбутися за допомогою анальгетиків. Інші ускладнення: жовчний перитоніт, сепсис, місцеве нагноєння, пневмоторакс, плеврит, підшкірна емфізема фіксуються вкрай рідко (менше 1 на 1000 випадків).
Трансюгулярна біопсія печінки є більш інвазивним методом, ніж біопсія крізь шкіру. Вона застосовується у пацієнтів з важкою коагулопатією. Процедура включає в себе канюлювання правої внутрішньої яремної вени і проведення катетера через верхню порожнисту вену в печінкову вену. Потім через печінкову вену в печінку вводиться тонка голка. Біопсія успішна більш ніж у 95% випадків. Рівень ускладнень низький, у 0,2% випадків розвивається кровотеча внаслідок пункції печінкової капсули.
Оцінювання ступеня вираженості фіброзних змін печінкової тканини за допомогою біопсії має серйозні обмеження, обумовлені об’єктивними і суб’єктивними причинами. До об’єктивних причин належить малий об’єм біоптату (зазвичай це 1/500000 частина тканини органу). Слід пам’ятати, що при наявності нерівномірно-дифузного ураження печінки різні сегменти можуть мати різні стадії фіброзу та індексу гістологічної активності. Порівняння результатів парних біопсій, отриманих з правої і лівої частки печінки пацієнтів, інфікованих вірусом HСV, показало, що розбіжність на 1 бал індексу гістологічної активності були в 25% випадків; у 14,5% пацієнтів, у яких по біопсії з однієї частки печінки був поставлений цироз печінки, по біопсії з іншої частки був виявлений виражений фіброз.
Отримання адекватного обсягу біоптата (довжиною близько 25мм із захопленням не менш ніж 11 портальних трактів) не гарантоване при доступі крізь шкіру. До суб’єктивних причин відмінностей у визначенні стадії фіброзу в одному і тому ж біоптаті відносять кваліфікацію морфолога.
При оцінці різними фахівцями-морфологами відмінності можуть спостерігатися до 20% випадків. Динамічне спостереження за фіброзом печінки за допомогою біопсії усладнене внаслідок описаних обмежень і інвазивності самого методу.
Біохімічні маркери для оцінки ступеню фіброзу
Іншим варіантом оцінки ступеню фіброзу, який потребує значно менших травматичних втручань у порівнянні з біопсією, є біохімічні маркери.
Незважаючи на те, що при розвитку фіброзу в печінці накопичуються різні типи колагену (тип I, III, IV, V, VI), саме колаген III типу, який є компонентом базальної мембрани, заслуговує на особливу увагу з кількох причин: його рівень відображає поточні гепатоцелюлярні пошкодження і дисфункції , колаген III грає важливу роль в гепатоцелюлярній регенерації лобулярної структури. Крім того, цей тип колагену синтезується в першу чергу при різних пошкодженнях печінки. При вірусному гепатиті рівень колагену III в сироватці збільшується відповідно до ступеня розвитку фіброзу. У пацієнтів, успішно пролікованих інтерфероном, рівень колагену III має тенденцію до зменшення. Колаген III, таким чином, може використовуватися як параметр оцінки антивірусної терапії.
Іншим маркером, який може використовуватись для визначеня ступеня фіброзу печінки є гіалуронова кислота – глікозаміноглікан, який грає важливу роль в сполучнотканинному матриксі. Її період напіврозпаду в нормі – 5 – 6 хв. Рівень гіалуронової килоти підвищується при захворюваннях, що характеризуються фіброзом і цирозом – зростає продукція, збільшується час напіврозпаду. Цей показник краще корелює зі ступенем гістологічного пошкодження печінки, ніж традиційні маркери: трансамінази, лужна фосфатаза, білірубін.
Тести на основі біохімічних показників
Необхідно враховувати порівняно невелику діагностичну цінність окремо взятих біохімічних показників для визначення ступеню фіброзу, оскільки на жаль, більшість з них не є органоспецифічними. Саме тому, з метою підвищення точності діагностики був запропонований ряд панелей, які використовують біохімічні показники(АСТ, АЛТ, ЛФ, ГГТП, загальний білірубін та ін.) та гострофазні білки (альфа-2-макроглобулин, гаптоглобін, феритин і ін.). Дискримінантні функції, які були отримані, спираючись на зміни цих показників, можуть відображати як активність процесу запалення в тканині органу, так і зміни його синтетичної функції, що дозволяє судити про стадії фіброзу.
Одним із найбільш простих та розповсюджених тестів є APRI тест: (aspartate aminotransferase to platelet ratio index) – індекс співвідношення АСТ / кількість тромбоцитів. Він був описаний у 2003 році і розраховується за спеціальною формулою:
APRI = АСТ * 100 / ((верхня межа АСТ) * тромбоцити (10 ^ 9 / л)
Якщо значення більше 1,0, то ймовірність значного фіброзу велика, якщо менше 0,5 – мала.
Точність цього тесту для діагностики фіброзу і цирозу підтверджена декількома дослідженнями. Значення індексу APRI 0,3 – 0,5 виключають виражений фіброз і цироз, а значення > 1,5 вказують на клінічно значущий фіброз (за шкалою METAVIR) у пацієнтів з хронічним вірусним гепатитом С. У пацієнтів з неалкогольним жировим захворюванням печінки значення APRI також мають тенденцію підвищуватися з підвищенням тяжкості фіброзу. При використанні APRI для початкового скринінгу може бути правильно діагностовано понад 50% пацієнтів з середніми рівнями фіброзу. У пацієнтів, інфікованих ВІЛ і ВГС, значення індексу APRI > 1,8 в 75% випадків вказували на виражений фіброз, а значення < 0,6 виключали фіброз в 87% випадків. Загалом, APRI тест досить простий, надійний і економічний, його застосування може дозволити приблизно зрозуміти наявність фіброзу високих стадій, спираючись на загальнодоступні показники, і може бути рекомендований в якості скринінгового обстеження.
Тест Forns був розроблений на основі обстеження 476 пацієнтів з хронічним гепатитом С, яким проводилася біопсія печінки. У формулі розрахунку використовуються параметри: холестерин, тромбоцити, вік, ГГТП. Формула розрахунку: Forns = 7.811 – 3.131 * ln (тромбоцити) + 0.781 * ln (ГГТП) + 3.467 * ln (вік) – 0.014 * (холестерин, мг / дл). Значення менше 4.2 відповідає відсутності фіброзу з ймовірністю 96%.
Тест FibroIndex розроблений в результаті обстеження 360 хворих на хронічний гепатит С. Використовуються параметри: тромбоцити, АСТ, гамма-глобулін. Формула розрахунку: FibroIndex = 1.738 – 0.0064 * Тромбоцити [* 10 ^ 4 / мл ^ 3] + 0.005 * АСТ [Од / л] + 0.463 * Гамма-глобулін [г / дл] Якщо значення менше 1.25, то ймовірність відсутності фіброзу вище 1 порядку 87%. Якщо значення більше 2.25, то ймовірність фіброзу більше 1– близько 90%.
Тест FIB-4 було розроблено на основі обстеження 832 пацієнтів з коінфекцією ВІЛ / HCV. Використовуються параметри: вік, АСТ, АЛТ, тромбоцити. Формула розрахунку: FIB-4 = вік (років) * АСТ / (тромбоцити (10 ^ 9 / л) * sqrt (АЛТ)) Якщо значення менше 1.45, то ймовірність значного фіброзу мала (порядку 90%). Якщо значення більше 3.25, то велика.
Тест MDA розроблено в результаті обстеження 455 хворих на хронічній гепатит С єгіптян. Використовують наступні параметри: альбумін, тромбоцити, лужну фосфотазу, АЛТ, АСТ. Формула розрахунку: MDA = [Альбумін (g / L) x0.3 + тромбоцити (10 (9) / L) x0.05] – [Лужна фосфотаза (IU / L) x0.014 + (Aст / АЛТ) x6 + 14 ] Імовірність наявності цирозу висока, якщо значення менше 0 (ймовірність біля 90%). Якщо значення більше 0, то велика ймовірність відсутності цирозу (теж близко 90%).
NAFLD Fibrosis Score (Шкала фіброзу при неалкогольний жировій хворобі печінки) заснована на шести доступних параметрах (вік, індекс маси тіла, гіперглікемія, рівень тромбоцитів, альбуміну, співвідношення АСТ / АЛТ) і розраховується за опублікованою формулою (http://nafldscore.com).
Іншим варіантом визначення ступеня фіброзу печінки є комерційні тести, засновані на біохімічних показниках, серед яких в Україні найбільш прозповсюдженим є Фібротест.
Фібротест і Актітест є результатом більш ніж десятирічних досліджень, проведених групою співробітників відділення гепатології та гастроентерології клініки Пиття-Сальпетрієр (Париж) під керівництвом проф. Тьєрі Пойнара. Тест запатентований. Придатність і аналітична стандартизація Фібротесту / Актітесту була встановлена у великий кількості клінічних випробувань.
Фібротест / Актітест відображає стадії фіброзу (F0, F1, F2, F3, F4) і ступінь некрозапального процесу (А0, A1, A2, А3) по міжнародній загальноприйнятій системі METAVIR, дозволяє здійснювати універсальну інтерпретацію результатів дослідження.
Складові Фібротесту наступні.Альфа-2-макроглобулін – білок гострої фази, який має досить широкий спектр активності, інгібітор ендопептідаз, утворюється в підшлунковій залозі. Він має здатність приєднувати і транспортувати багато відомих цитокінів (інтерлейкіни, інтерферони, фактори некрозу пухлини, стимуліни, інгібін і фактори росту). Кожна його субодиниця може слугувати «пасткою» для будь-якого з протеолітичних ферментів. При цьому протеїнази зберігають свою активність, перебуваючи в «пастці». Період напіввиведення такого комплексу з системи кровообігу не перевищує 1-2 хв, і в цей період протеїнази продовжують виконувати свої функції. Таким чином альфа-2-макроглобулін регулює велику кількість функцій організму, пов’язаних з системою крово- і лімфообігу. У печінці здійснюється його розпад, внаслідок якого активуються зірчасті клітини і таким чином стимулюється фіброгенез.
Гаптоглобін – глікопротеїн плазми крові, що специфічно зв’язує гемоглобін, синтезується в печінці. Гаптоглобін належить до білків гострої фази. Підвищення його рівня в крові відбувається внаслідок стимуляції інтерлейкінами клітин печінки. Цей показник має негативний кореляційний зв’язок зі ступенем фіброзу печінки.
Аполіпопротеїн А1 генерується тканиною печінки і виконує транспортні функції по відношенню до холестерину. Велика його кількисть міститься у екстрацелюлярному матриксі, і його рівень знижується з ростом стадії фіброзу.
Загальний білірубін утворюється при розпаді гемоглобіну в клітинах ретикулоендотеліальної системи, особливо активно в селезінці, а також в купферовських клітинах печінки. Підвищення його рівня служить проявом печінково-клітинної недостатності.
Гамма-глутамілтранспептидаза – чутливий, але неспецифічний індикатор ураження жовчних канальців. Найбільш високі концентрації виявляються в епітеліальних клітинах жовчних канальців, таким чином підвищення рівня гамма-глобуліну є ознакою фіброзу, обумовленого ураженням канальцевої системи печінки.
Аланінамінотрансфераза – найчутливіший і найспецифічніший індикатор гепатоцелюлярного пошкодження (запалення і некроз клітин), локалізується в цитоплазмі гепатоцита.
Фібротест не слід використовувати при гострих гепатитах. Хибнопозитивні результати Фібротесту / Актітесту найчастіше пояснюються підвищенням білірубіну через причини, не пов’язані з хронічним гепатитом (синдром Жильбера, гемоліз або підпечінковий холестаз (пухлина, жовчнокам’яна хвороба) або ліки (лікування рибавірином). В окремих випадках підпечінкового холестазу може спостерігатися ізольоване підвищення ГГТП при нормальних значеннях білірубіну. Зниження концентрації гаптоглобіну в результаті вираженого гемолізу (наявність протезу серцевого клапана, прийом рибавірину) також може призводити до хибнопозитивних результатів Фібротесту. Ризик хибнопозитивних результатів може виникати при загостренні хронічних запальних процесів. Наприклад, деякі запальні стани супроводжуються збільшенням рівня гаптоглобіну, тому що він є IL-6-залежним білком гострої фази. При цьому кріоглобулінемічний васкуліт або запальні прояви при ВІЛ-інфекції не супроводжуються зміною концентрації гаптоглобіну.
Для більш поглибленого дослідження уражень печінки може використовуватись тест Фібромакс.
Фібромакс є тестом, який складається з 5 розрахункових алгоритмів і виконується за результатами алгоритмічного опрацювання десяти біохімічних показників: альфа-2-макроглобуліну, гаптоглобіну, аполіпопротеїну А1, ГГТ (гамма глютамілтрансферази), загального білірубіну, АЛТ, АСТ, тригліцеридів, загального холестерину і глюкози.
Фібромакс спрямований на діагностику важкості перебігу різноманітних уражень печінки: ступеня тяжкості фіброзу печінки з перекладом в систему METAVIR – Фібротест (FibroTest); активності некрозапального процесу в печінці – АктіТест (ActiTest). Крім того, Фібромакс додатково дозволяє діагностувати жирову дистрофію (стеатоз) печінки – СтеатоТест (SteatoTest); алкогольний стеатогепатит у осіб, що зловживають спиртними напоями – ЕшТест (AshTest); неалкогольний стеатогепатит у пацієнтів з ожирінням, резистентністю до інсуліну, гіперліпідемією, а також у пацієнтів із цукровим діабетом – НешТест (NashTes).
Методи інструментальної діагностики степеня фіброзу печінки
Еластографія – інструментальний, неінвазивний метод дослідження, який дозволяє за короткий проміжок часу (5-7 хвилин) визначити ступінь фіброзу печінки у пацієнтів з хронічними захворюваннями цього органу будь-якої етіології. За варіантами проведення еластографію можна поділити на транзієнтну та зсувнохвильову.
Методика транзієнтної еластографії для визначення ступеня фіброзу або наявності цирозу печінки застосовує індуковані механічні коливання низької частоти і амплітуди, які викликають у печінці еластичну хвилю зрушення – її швидкість прямо пропорційна ступеню фіброзної трансформації органу. Швидкість проходження еластичних хвиль по печінці оцінюється за допомогою ультразвуку. Обробка отриманої інформації відбувається із застосуванням алгоритму, що враховує еластичність печінки здорових людей, яка служить точкою відліку. Отримана величина еластичності печінки виражається в кілопаскалях (кПа) і, згідно з даними літератури, має виражений зв’язок з результатами гістологічного дослідження по системі METAVIR.
Для проведення транзієнтної еластометрії існують деякі обмеження: процедура не рекомендована пацієнтам з кардіостимуляторами, пацієнтам з асцитом, вагітним жінкам через високу акустичну потужність імпульсу, межа глибини вимірювання складає 5 cм з фіксованим розміром контрольного об’єму 4 cм.
Діагностична точність досить висока і має наступні показники:
- перипортальній фіброз (F1) – 78%;
- портопортальний фіброз (F2) – 84%;
- портоцентральний фіброз (F3) – 86%;
- цироз печінки (F4) – 89%.
Зсувнохвильова еластографія не потребує зовнішньої компресії тканин ультразвуковим датчиком. Напруження в тканинах створюються ультразвуковими пучками хвиль.
Проведення процедури нагадує звичайне ультразвукове обстеження органів черевної порожнини і потребує такої самої підготовки – пацієнт повинен бути натщесерце, кишечник пацієнта повинен містити мінімальну кількість газу. Час проведення процедури зазвичай складає 15- 20 хв. Враховуючи, що дослідження проводиться в режимі реального часу, це дозволяє безпосередньо візуалізувати печінку пацієнта, і зробити вимірювання посегментарно, маючи можливість приділити більшу увагу при виявленні якихось зовнішніх змін.
При звичайному ультразвуковому обстеженні печінки практично неможливо визначити наявність і вираженість фіброзу.
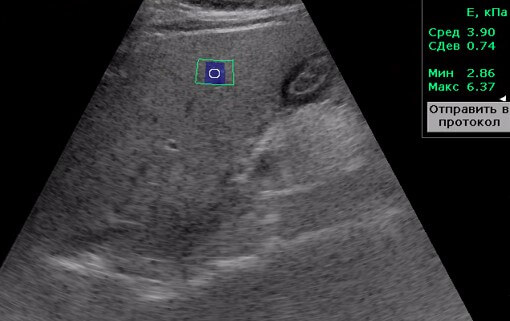
Так, на продемонстрованій сканограммі показник жорсткості печінкової тканини складає 3,9 кПа із похибкою вимірювання 0,74, що відповідає F0 за METAVIR.
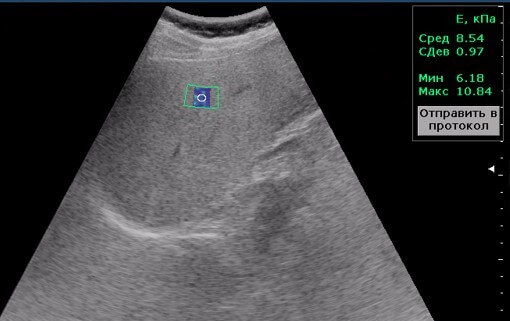
У той же час, при відсутності зовнішніх відмінностей у режимі сірої шкали, еластометричний показник жорсткості паренхіми печінкової тканини цього пацієнта складає 8,54 кПа із похибкою вимірювання 0,97, що відповідає F2 за METAVIR.
Необхідно підкреслити, що останнім часом в процедуру визначення ступеня фіброзу печінки за допомогою зсувнохвильової еластометрії включають вимірювання еластичності селезінки, як ранній маркер портальної гіпертензії.
За умови відсутності на ультразвуковому апараті модуля еластометрії, можливе використання непрямих методів вимірювання еластичності печінки для оцінки ступеня її фіброзу. Одним із можливих варіантів є визначення швидкості кровотоку в портальній системі за допомогою доплерографічних досліджень. Метод заснований на можливості оцінити артеріальний кровотік у печінці в систолу і діастолу. Так, якщо систолічний кровотік насамперед залежить від серцевого викиду, то діастолічний багато в чому визначається внутрішньоорганним судинним опором. Прогресування фіброзу супроводжується зростанням тиску в системі ворітної вени і, відповідно, збільшенням опору току крові по селезінковій артерії. Найбільш інформативним показником для діагностики вираженості фіброзу вважають пульсатівний індекс селезінкової артерії.
Одним із найбільш сучасних методів, який дозволяє відтворити фіброзні зміни печінки у форматі 3D в реальному часі, є МРТ-еластографія
Затверджена FDA в 2009 році, МРТ-еластографія є неінвазивним, високочутливим методом для визначення рівня фіброзних змін печінки за допомогою використання низькочастотних механічних коливань. Більшість сучасних апаратів МРТ за потребою можуть бути дооснащені модулем для проведення еластографії.
Після установки цей інструмент генерує 60 Гц хвилі через пластикову трубку в невеликому пластиковому барабані, розміщеному на животі пацієнта. Повільний рух розповсюдження хвилі корелює з більш високою жорсткістю тканини печінки. Стандартні зображення МРТ вловлюють незначні рухи тканини, і, за допомогою спеціального алгоритму перетворюють дані в кольорові шкали зображення, які відповідають рівню жорсткості паренхіми печінки.
Лікування фіброзу печінки
Що ж стосується лікування фіброзу печінки, необхідно пам’ятати декілька основних правил
Враховуючи, що фіброзні зміни печінкової тканини є наслідком хронічного ушкодження печінки, в першу чергу необхідна активна терапія захворювання, яке його викликало, що в свою чергу, призведе до поступового зменшення та зникнення запального процесу в печінці. Необхідним є усунення вірусів гепатиту В і С при хронічних вірусних гепатитах, утримання від споживання алкоголю при алкогольній хворобі печінки, виведення заліза при гемохроматозі або міді при хворобі Вільсона, при біліарній обструкції обов’язковою умовою є декомпресія жовчних проток. Такі процедури можуть зупинити розвиток фіброзу, а у деяких пацієнтів сприяти усуненню певних фіброзних змін.
Препарати, які використовуються для регрессії фіброзу, зазвичай є дуже токсичними для тривалого використання (наприклад, кортикостероїди, пеніциламін) або не мають доведеної ефективності (наприклад, колхіцин). Ефективність інших антифібротичних агентів поки вивчається. Популярною альтернативою є Силімарин – досить безпечний (за винятком випадків, коли він поєднується з деякими препаратами для лікування гепатиту С), але не має високої ефективності для лікування цієї патології.
Використана література:
Karsdal, MA, Daniels, SJ, Holm Nielsen, S, et al. Collagen biology and non‐invasive biomarkers of liver fibrosis. Liver Int. 2020; 40: 736– 750. https://doi.org/10.1111/liv.14390.
Orasan OH, Ciulei G, Cozma A, Sava M, Dumitrascu DL. Hyaluronic acid as a biomarker of fibrosis in chronic liver diseases of different etiologies. Clujul Med. 2016;89(1):24-31. doi:10.15386/cjmed-554.
Forns X, Ampurdanès S, Llovet JM, Aponte J, Quintó L, Martínez-Bauer E, Bruguera M, Sánchez-Tapias JM, Rodés J. Identification of chronic hepatitis C patients without hepatic fibrosis by a simple predictive model. Hepatology. 2002 Oct;36(4 Pt 1):986-92. doi: 10.1053/jhep.2002.36128. PMID: 12297848.
Koda M, Matunaga Y, Kawakami M, Kishimoto Y, Suou T, Murawaki Y. FibroIndex, a practical index for predicting significant fibrosis in patients with chronic hepatitis C. Hepatology. 2007;45:297–306.
Sterling RK, Lissen E, Clumeck N, Sola R, Correa MC, Montaner J, S Sulkowski M, Torriani FJ, Dieterich DT, Thomas DL, Messinger D, Nelson M; APRICOT Clinical Investigators. Development of a simple noninvasive index to predict significant fibrosis in patients with HIV/HCV coinfection. Hepatology. 2006 Jun;43(6):1317-25. doi: 10.1002/hep.21178. PMID: 16729309.
Attallah AM, Shiha GE, Omran MM, Zalata KR. A discriminant score based on four routine laboratory blood tests for accurate diagnosis of severe fibrosis and/or liver cirrhosis in Egyptian patients with chronic hepatitis C. Hepatol Res. 2006 Mar;34(3):163-9. doi: 10.1016/j.hepres.2005.12.004. Epub 2006 Feb 14. PMID: 16478676.
www.biopredictive.com











