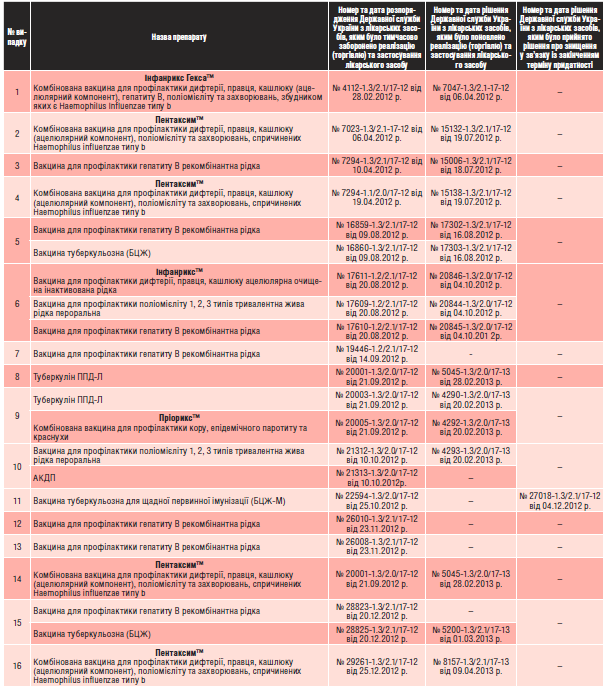
 У таблиці представлено препарати, застосування яких було тимчасово призупинено через реєстрацію випадків НППІ (летальні випадки) у післявакцинальному періоді.
У таблиці представлено препарати, застосування яких було тимчасово призупинено через реєстрацію випадків НППІ (летальні випадки) у післявакцинальному періоді.
(Продовження. Початок див. у «ВЗ» № 21-22 від 31.05.2013 р.)
Період розслідування повинен тривати не більше 30 діб з моменту реєстрації випадку. При розслідуванні здійснюється аналіз низки даних, що можуть відігравати вирішальну роль у виникненні смерті/госпіталізації щепленого та допомогти визначити її причину. Аналізуються дані анамнезу життя, перенесених захворювань, щеплювального анамнезу, результати медичного огляду перед щепленням, епідеміологічне оточення, відповідність дотримання медичним показанням та протипоказанням щодо щеплення, процедурі імунізації. Також аналізуються: умови температурного режиму зберігання та транспортування вакцин, анатоксинів та алергену туберкульозного, оперативна інформація щодо кількості використаних доз підозрюваної серії вакцини по ЛПЗ/району/області, наявність або відсутність зареєстрованих післявакцинальних реакцій/ускладнень, їх частота.
Після проведення розслідування група оперативного реагування надає до Департаменту Центру попередню довідку за результатами проведеного розслідування.
Після отримання результатів лабораторних та інструментальних досліджень (при госпіталізації) чи даних патологоанатомічного діагнозу з результатами гістологічних, вірусологічних, бактеріологічних, токсикологічних досліджень (у разі летального випадку), не пізніше 30 днів з моменту реєстрації випадку, група оперативного реагування встановлює або спростовує зв’язок патологічного стану з проведеним щепленням або туберкулінодіагностикою та надає заключний висновок (додаток 2 Положення про оперативне реагування на несприятливі події після імунізації при застосуванні вакцин, анатоксинів та алергену туберкульозного у разі госпіталізації або летального випадку (Наказ МОЗ України від 16.09.2011 р. № 595) до Департаменту Центру.
Як диференціювати ускладнення після вакцинації з іншими захворюваннями
Порушення стану здоров’я, що виникають після вакцинації, не слід одразу відносити до побічної реакції, доки не буде встановлено її причинно-наслідковий зв’язок зі щепленням. Хоча батьки першими спостерігають за розладами здоров’я щепленого, однак лише лікар може встановити причину їх розвитку. Це має велике значення для встановлення правильного діагнозу та призначення своєчасного й адекватного лікування.
Відомо, що переважна кількість щеплень припадає на перший рік життя дитини. Таким чином, дитина весь цей проміжок часу знаходиться у післявакцинальному періоді. При цьому не виключено, що у цей час дитина може хворіти гострими респіраторними захворюваннями та іншими хворобами інфекційного чи неінфекційного ґенезу. Приєднання будь-яких захворювань може спостерігатися у різні проміжки післявакцинального періоду. Тому будь-яке захворювання у післявакцинальному періоді може бути розцінено, як можлива побічна реакція (реакція/ускладнення) на введення вакцини. Отже необхідно проводити збір анамнезу та диференційну діагностику між побічними реакціями на щеплення та захворюваннями, які лише у часі пов’язані з імунізацією. Особливо важливо виключити у щепленого наявність таких захворювань як менінгіт, сепсис, пневмонія, наявність екстреної хірургічної патології, оскільки зволікання їх лікування є небезпечним для життя.
Лише у разі виключення ролі інших чинників у погіршенні стану здоров’я щепленого слід розглядати питання про його зв’язок зі щепленням. При вирішені цього питання важливо враховувати час виникнення патологічних клінічних проявів та його співвідношення з проведеним щепленням.
Коли йдеться про виникнення побічних реакцій, то в основному вони пов’язані з індивідуальними особливостями імунної відповіді організму на щеплення та властивостями вакцини. У переважній більшості післявакцинальні реакції мають місцеві та/або загальні прояви. Місцевими проявами можуть бути гіперемія, інфільтрат, набряк та болючість у місці введення вакцини. Вони спостерігаються одразу після введення вакцин як живих, так і інактивованих та тривають протягом декількох діб. Загальні реакції проявляються підвищенням температури тіла, головним болем, порушенням сну, апетиту тощо, як правило їх тривалість становить від 1 до 3 діб.
Для живих та інактивованих вакцин існують характерні клінічні прояви післявакцинальних реакцій та строки їх розвитку. Так для інактивованих вакцин загальні реакції реєструються у перші 72 години, а для живих вакцин — не раніше, ніж через 4-5 діб від моменту щеплення.
Вичерпний перелік можливих проявів побічних реакцій та строки їх розвитку наведені в інструкціях про застосування вакцини (далі — інструкція) відповідної вакцини/анатоксину/алергену туберкульозного та у додатках 1,2 Інструкції щодо організації епідеміологічного нагляду за несприятливими подіями після імунізації при застосуванні вакцин, анатоксинів та алергену туберкульозного, затвердженої наказом МОЗ України від 16.09.2011 р. № 595.
Можливі причини летальних наслідків вакцинації
Особливої уваги заслуговує розгляд питання причин летальних випадків у післявакцинальному періоді, коли існує зв’язок між смертю щепленого і використанням вакцини. Однак слід зазначити, що у певних випадках такого наслідку можна було б уникнути, а в інших — ні.
До останніх належать особливості індивідуальної відповіді організму на введення вакцини та виникнення реакції гіперчутливості до будь-якого компоненту вакцини. Для запобігання цьому перед щепленням збирається анамнез життя відповідно до п. 10 «Положення про організацію і проведення
профілактичних щеплень та туберкулінодіагностики» (Наказ МОЗ України від 16.09.2011 р. №595). За імунізованою особою у закладі охорони здоров’я, де відбулося щеплення, повинно здійснюватися спостереження протягом 30 хвилин після вакцинації, оскільки цей проміжок часу є найбільш небезпечним щодо виникнення реакцій гіперчутливості (п. 16 «Положення про організацію і проведення профілактичних щеплень та туберкулінодіагностики» (Наказ МОЗ України від 16.09.2011 р. №595). У разі виникнення реакції гіперчутливості щепленому своєчасно надається невідкладна медична допомога відповідно до затвердженого МОЗ протоколу.
Серйозним ускладненням при введенні вакцини є розвиток інфекційно-токсичного шоку, який може мати летальні наслідки та пов’язаний із застосуванням вакцини. Зазвичай причиною такого ускладнення є медична помилка, коли розведена напередодні жива вакцина використовується наступного дня, що є категорично неприпустимим. Згідно з інструкцією живу вакцину в мультидозових флаконах можна використати після розведення (відновлення) лише протягом 6-8 годин. Зберігати таку вакцину необхідно лише у холодильнику за температури +2…+8°С. В кінці робочого дня розведена жива вакцина повинна бути знищена. Порушення зазначених правил може коштувати життя щепленого.
Також причиною смерті у післявакцинальному періоді, що пов’язана з використанням вакцини, може бути розведення її розчинником, що не входить до комплекту. Наприклад, використання в якості розчинника будь-яких лікарських засобів у рідкій лікарській формі. У літературі описані випадки використання у якості розчинника інсуліну та нейролептику. Такі події розцінюються як медична помилка і їх можна уникнути за дотримання медичними працівниками вимог інструкції про застосування вакцини.
У наступній публікації ми наведемо інформацію, яка демонструє реальні клінічні ситуації, що виникли у післявакцинальному періоді, та їх аналіз, проведений групами оперативного реагування на несприятливу подію після імунізації.
Оксана САХНЮК, директор Департаменту медичних імунобіологічних препаратів та імунопрофілактики ДП «Державний експертний центр МОЗ України»
Олена МАТВЄЄВА, директор Департаменту післяреєстраційного нагляду ДП «Державний експертний центр МОЗ України»
Ганна МОЙСЕЄВА, заступник директора Департаменту медичних імунобіологічних препаратів та імунопрофілактики ДП «Державний експертний центр МОЗ України»
Валерія ВАСИЛЬЄВА, начальник відділу клінічних випробувань та моніторингу МІБП Департаменту медичних імунобіологічних препаратів та імунопрофілактики ДП «Державний експертний центр МОЗ України»
Тетяна БАШКАТОВА, провідний фахівець відділу клінічних випробувань та моніторингу МІБП Департаменту медичних імунобіологічних препаратів та імунопрофілактики ДП «Державний експертний центр МОЗ України»











